美国食物药品治理局(FDA)曾经估计,到2025年,FDA每一年将核准10~20款细胞与基因医治(CGT)产物。麦肯锡近期的一份陈诉则基在管线进展作出更斗胆的猜测:仅于2024年,估计将有多达21种细胞疗法及多达31种基因疗法得到FDA核准。
这些预言可否实现?“这只是行将到来的海潮的第一波。”美国再生医学同盟(ARM)首席履行官Timothy Hun于年头发表的一篇文章中对于此暗示十分乐不雅。近五年来,得到FDA核准的CGT产物数目连续增加,2022年更是全世界CGT产物获批总数创纪录的一年。当前这一范畴有跨越2000项临床实验正于开展,此中跨越100项已经迈入Ⅲ期。
按照已经公然信息和ARM猜测信息,至2023年底,全世界规模内将有16款CGT产物有望初次获批上市或者迎来主要羁系进展(此中1款已经在3月份于日本获批上市)。
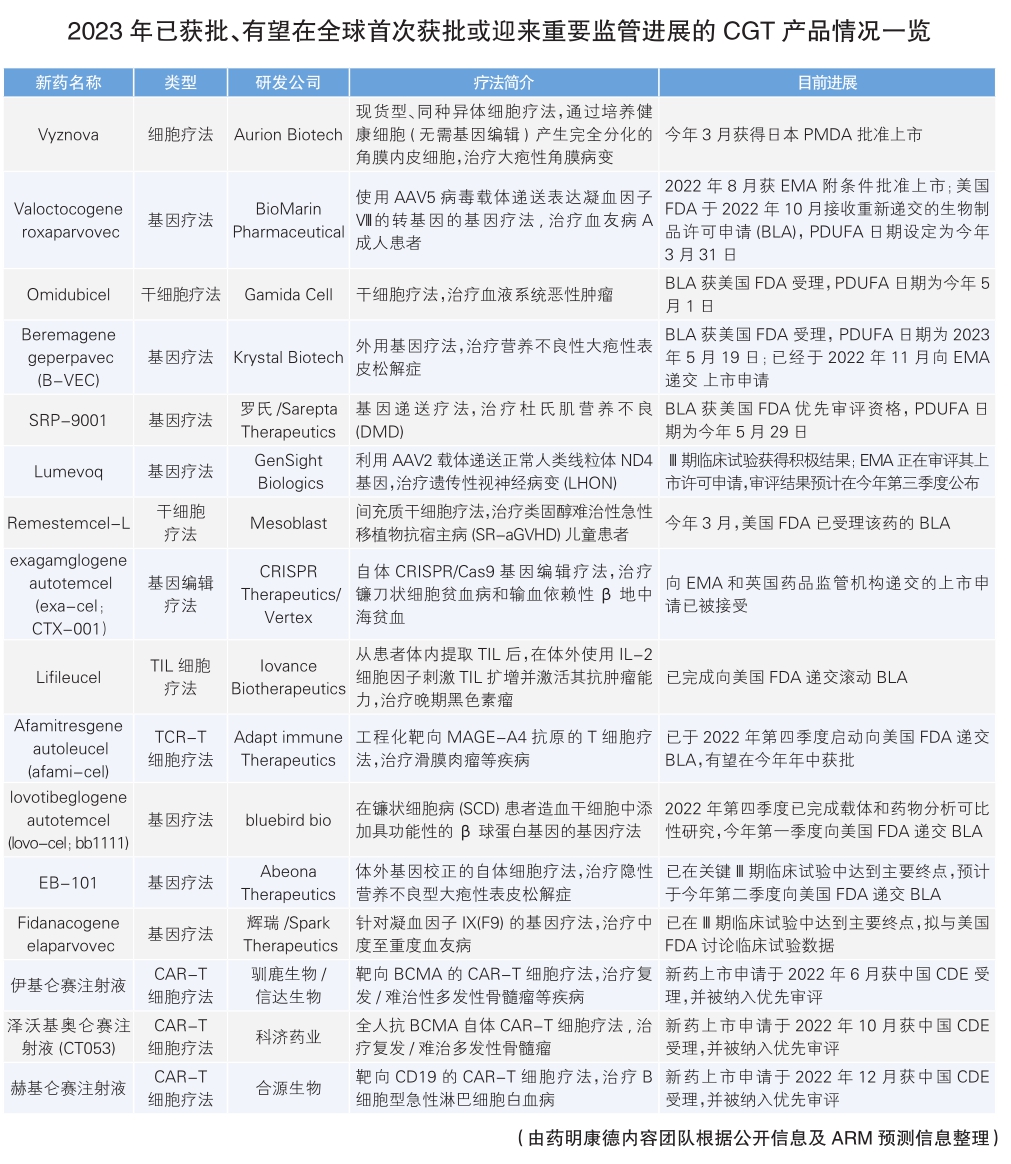
这些产物从疗法类型来看,包括7款基因疗法、1款基因编纂疗法、3款CAR-T细胞疗法、1款TCR-T细胞疗法、2款干细胞疗法、1款TIL疗法及1款同种异体细胞疗法。
于顺应证方面,这些候选基因疗法中一半针对于血液体系遗传疾病,CAR-T疗规则集中于血液肿瘤范畴。
就羁系进展而言,截至3月27日,已经有1款疗法得到日本医药品医疗器械综合机构(PMDA)核准上市;5款疗法已经公然明确PDUFA日期(即FDA完成新药上市申请审评的截止日期,凡是为自收到申报日起10个月,得到优先评审的缩短至6个月)或者欧洲药品治理局(EMA)审评成果预期宣布时间;2款疗法的上市申请已经被泰西羁系机构受理;3款CAR-T疗法的上市申请已经得到中国国度药监局药品审评中央(CDE)受理并被纳入优先审评,还有有5款疗法已经向泰西药品羁系机构递交上市申请或者明确推进上市规划。
于投融资方面,据不彻底统计,于CGT范畴,2023年有33家公司完成投融资勾当,共计融资跨越12亿美元。投融资事务数量及投融资数额于3月份到达本年的新高。
于细胞疗法范畴,共计24家公司得到融资,年夜部门专注在开发基因工程革新的免疫细胞疗法。此中,CARGO Therapeutics公司及Synthekine公司别离完成2亿及1亿美元的融资,于所有公司中压倒一切。这两家公司的配合的地方都于在解决第一代CAR-T细胞的局限,开发下一代CAR-T细胞疗法。CARGO Therapeutics公司的CD22靶向的CAR-T疗法CRG-022旨于降服肿瘤经由过程抗原丢掉孕育发生的耐药性。它已经经于Ⅰ期临床实验中让跨越50%已经经对于CD19靶向CAR-T疗法耐药的年夜B细胞淋巴瘤(LBCL)患者得到连续减缓。基在这一成果,FDA已经经授予它冲破性疗法认定。
Synthekine公司的SynCAR-001于表达靶向CD19的嵌合抗原受体以外,还有表达工程化革新的IL-2受体β亚基,于该公司设计的IL-2细胞因子的刺激下,可以加强CAR-T细胞扩增及长期性,同时降低最初的CAR-T细胞疗法剂量,减轻疗法毒副作用。
于基因疗法方面,本年一季度得到融资的11家公司(含两家同时开发细胞疗法的公司)中,虽然年夜部门聚焦在开发基在腺相干病毒载体的传统基因疗法,可是得到融资至多的两家公司均于开发传统基因疗法之外的立异医治模式。
本年年头完成1.75亿美元B轮融资的Metagenomi公司利用人工智能,从年夜天然中发明自然核酸酶,再革新天生基因编纂疗法。Metagenomi已经经测试了数百种新的基因编纂东西,并验证了实在用性。该公司开发的基因编纂东西包括CRISPR基因编纂体系、超小型碱基编纂体系,以和CRISPR相干转座酶(CAST)体系,该体系可将年夜段DNA精准插入基因组。(药明康德内容团队供稿)

2月份中美欧核准上市新药盘货 我国自立研发的三款新药于全世界规模内初次获批上市
2月份,中美欧核准上市的新药中,中国核准的新药数目至多,为5款;美国核准4款;欧盟核准3款新药上市。中国核准5款新药上市2月份,我国共核准5款新药上市(详见表1)。按照Pharmadigger数据库 2026-04-03 09:59
技能与人力的瓜葛并不是替换而是共生 制药行业将从智能制造迈向人机协同及绿色可连续成长
思惟,于高度智能化基础上,越发夸大“以报酬中央”与可连续成长。简言之,Pharma4.0聚焦效率晋升与主动化普和,而Pharma5.0则描绘了一幅人机协同、绿色低碳的将来制药新图景。Pharma5.0的焦点... 2026-03-30 15:24-米兰·(milan)




























 粤公网安备 44011202003184号
粤公网安备 44011202003184号