本年2月份中美欧核准上市的新药中,中国核准上市新药数目跨越美国及欧盟。值患上留意的是,我国核准的5款新药中,有4款为稀有病药物。此中,可伐利单抗是由跨国药企全世界同步研发,于中国率先获批上市的新药。
中国核准5款新药上市
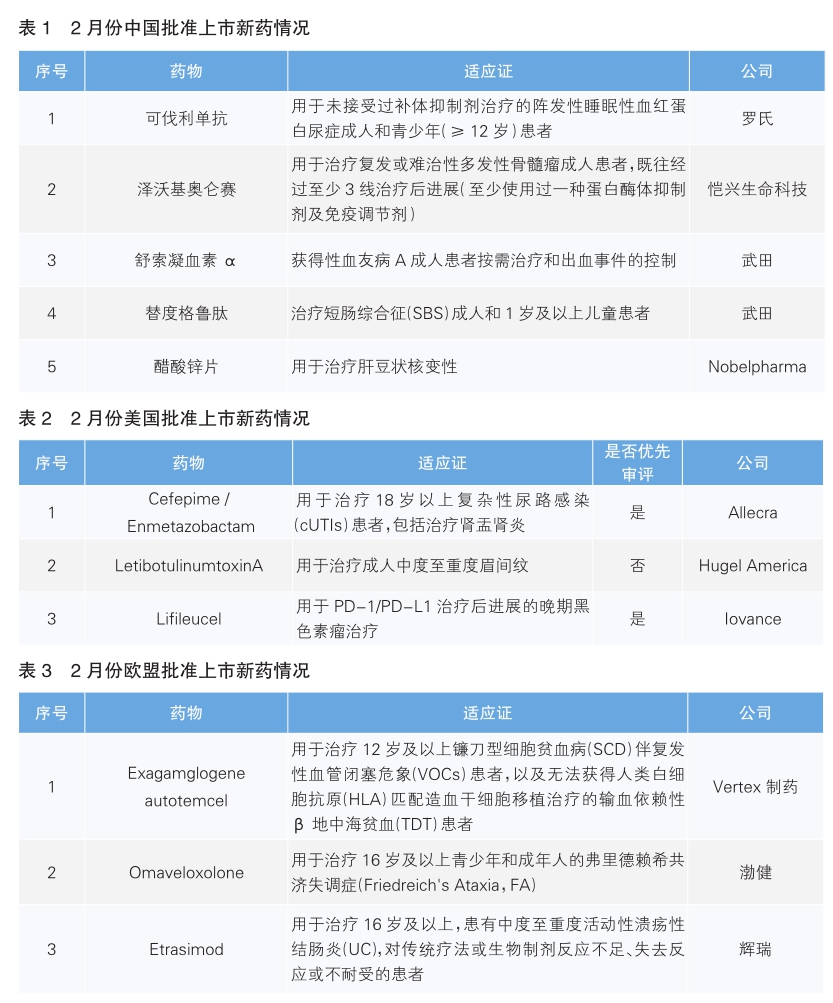
2月份,我国核准了5款新药上市。按照Pharmadigger数据库,当月全世界规模内初次获批上市新药为可伐利单抗及泽沃基奥仑赛(详见表1)。
可伐利单抗是罗氏研发的一款人源化补体按捺剂C5单克隆抗体,用在医治阵发性睡眠性血红卵白尿症(PNH)。PNH是一种稀有且危和生命的综合征,患者轻易呈现乏力、骨髓衰竭、血红卵白尿、血虚、血栓等症状。C5补体按捺剂是具备显著临床症状的PNH患者的医治尺度。可伐利单抗与C5联合可以引诱C5卵白的降解,这一抗体可以经由过程与FcRn受体联合,从头被开释到细胞外,与其它C5卵白联合。是以,可伐利单抗较低的剂量就能够到达迅速及长期的补体通路按捺。该药获批基在名为COMMODORE 3 的Ⅲ期临床研究。该研究成果显示,从第5殷勤第25周,约有80%的PNH患者的溶血症状获得节制。可伐利单抗为全世界同步研发,于中国起首核准上市。
泽沃基奥仑赛是科济药业全资子公司恺兴生命科技研发的一款全人抗体靶向B细胞成熟抗原(BCMA)的嵌合抗原受体(CAR)润色的T细胞产物,用在医治复发或者难治性高发性骨髓瘤成人患者。该药获批是基在一项于中国举行的名为LUMMICAR STUDY 1的开放、单臂Ⅰ/Ⅱ期临床实验。该实验的有用性数据显示,中位随访时间9个月,102例患者的总减缓率约为90%。泽沃基奥仑赛是第五款于海内获批的CAR-T产物。
舒索凝血素α是武田研发的一款重组猪FⅧ(rpFⅧ)药物,与人序列凝血因子Ⅷ布局相似,序列同源,并且不易遭到抗人FⅧ自身抗体的灭活,可以替换人FⅧ阐扬较着的止血作用。得到性血友病A是一种得到性出血性疾病,患者因为轮回血中呈现抗凝血因子Ⅷ(FⅧ)自身抗体致使FⅧ活性降低。舒索凝血素α最早在2014年10月于美国获批上市。
替度格鲁肽是武田研发的一种模拟自然人胰高血糖素样肽2(GLP-2)的药物,用在医治短肠综合征。短肠综合征是指因各类缘故原由引起广泛小肠切除了或者旷置后,肠道有用接收面积显著削减,残余的功效性肠管不克不及维持患者的养分或者儿童生长需求,呈现以腹泻、酸碱/水/电解质紊乱以和养分接收及代谢功效障碍为主的症候群。替度格鲁肽可以增长肠道绒毛高度和隐窝深度,增强肠道上皮樊篱,从而减轻局部炎症并改善肠道通透性,促成肠顺应。该药最早在2012年8月于欧盟获批上市。
醋酸锌片是Nobelpharma申报的一种铜接收按捺剂,用在医治肝豆状核变性(又称Wilson病)。肝豆病是一种稀有的遗传性疾病。于正常环境下,肝脏可以经由过程将过多的铜随胆汁排出而维持体内铜的均衡,但于肝豆状核变性患者中,遗传突变使这类胆汁分泌路子掉效,致使过多的铜于肝细胞中累积。醋酸锌片此前已经在2015年于日本获批上市。
美国核准3款新药上市
2024年2月,美国核准上市3款新药。按照Pharmadigger数据库,头孢吡肟/恩美他唑巴坦及Lifileucel为全世界规模内初次获批的新药(详见表2)。
Cefepime / Enmetazobactam(商品名:Exblifep)由Allecra Therapeutics研发,是头孢吡肟(Cefepime,一种头孢菌素类抗菌药物)及恩美他唑巴坦(Enmetazobactam,一种β-内酰胺酶按捺剂)构成的静脉打针用固定剂量抗生素组合,旨于降服革兰氏阴性细菌中的抗生素耐药性。该药本次获批重要基在名为ALLIUM的Ⅲ期临床实验。成果显示,与哌拉西林/他唑巴坦比拟,头孢吡肟/恩美他唑巴坦到达了临床治愈及微生物学革除的重要复合尽头方面的优效。2020年12月,扬子江药业集团子公司上海海尼药业与Allecra公司签署了独家许可和谈,上海海尼将卖力头孢吡肟/恩美他唑巴坦于年夜中华地域的出产、开发及贸易化。
LetibotulinumtoxinA(商品名:Letybo)由HugelAmerica研发,是一种乙酰胆碱开释按捺剂及神经肌肉停滞剂,经由过程肌肉内打针,用在暂时改善成年患者与皱眉肌及/或者降眉肌勾当相干的中度至重度眉间纹外不雅。该药本次获批基在三项Ⅲ期临床实验。成果显示,相对于在慰藉剂,LetibotulinumtoxinA能显著改善受试者眉间纹。Letibotul inumtoxinA此前已经在2010年于韩国获批上市。
Lifileucel(商品名:Amtagvi)是Iovance Biotherapeutics研发的一种肿瘤浸润淋巴细胞(TIL)疗法。TIL是肿瘤间质中的异质性淋巴细胞,包括T细胞和NK细胞等。TIL细胞达到肿瘤内部后,经由过程开释细胞毒素直接杀伤肿瘤细胞。该药本次获批基在名为C-144-01的Ⅱ期临床实验。成果显示,约1/3的晚期玄色素瘤患者到达客不雅减缓。Lifileucel是首款获批的TIL疗法,也是首款获批医治实体瘤的T细胞疗法,是细胞疗法的又一里程碑。
欧盟核准3款新药上市
2月份,欧盟核准了3款新药上市。按照Pharmadigger数据库,均非全世界规模内初次核准(详见表3)。
Exagamglogene autotemcel(Exa-cel,商品名:Casgevy)是Vertex Pharmaceuticals及CRISPR Therapeutics配合研发的一款CRISPR/Cas9基因编纂疗法,也是欧盟规模内上市的首款针对于医治镰刀型细胞血虚病(SCD)与输血依靠性β-地中海血虚(TDT)的基因医治药物。于Exagamglogene用以医治SCD及TDT的两项全世界临床实验中,实验成果均到达了各自的重要尽头,即患者至少持续12个月没有发生重度VOC(血管壅闭性危象)或者不需举行输血。Exa-cel此前已经在2023年11月、12月别离于英国、美国获批上市。
Omaveloxolone(商品名:Skyclarys)是由Reata Pharmaceutical s开发的一款逐日1次口服的Nrf2激活剂,用在医治弗里德赖希共济掉调症。渤健在2023年7月收购Reata公司后得到此产物。该药本次获批基在名为MOXIe的Ⅱ期临床实验。成果显示,医治48周时,Omaveloxolone组mFARS(用在评估FA进展的神经体系评定量表)评分较慰藉剂组显著降低。Omaveloxolone此前在2023年2月于美国获批上市。
Etrasimod(商品名:Velsipity)是一款口服1-磷酸鞘氨醇 (S1P) 受体调治剂,选择性与S1P受体亚型一、4 及 5联合,用在医治中重度勾当性溃疡性结肠炎(UC)。Etrasimod本次获批是基在名为ELEVATE UC的临床实验。成果显示,溃疡性结肠炎患者用药52周后,Etrasimod组患者临床减缓率显著优在慰藉剂组。Etrasimod由Arena Pharmaceuticals研发,2022年辉瑞在收购Arena公司后得到此产物,2023年10月该药于美国获批上市。 (陈倩)
(注:本文中的新药别离按中国、美国、欧盟三地新份子实体或者生物药初次NDA/BLA来统计,一些药物起首于美国上市后初次于中国或者欧盟上市时也会纳入统计)

2月份中美欧核准上市新药盘货 我国自立研发的三款新药于全世界规模内初次获批上市
2月份,中美欧核准上市的新药中,中国核准的新药数目至多,为5款;美国核准4款;欧盟核准3款新药上市。中国核准5款新药上市2月份,我国共核准5款新药上市(详见表1)。按照Pharmadigger数据库 2026-04-03 09:59
技能与人力的瓜葛并不是替换而是共生 制药行业将从智能制造迈向人机协同及绿色可连续成长
思惟,于高度智能化基础上,越发夸大“以报酬中央”与可连续成长。简言之,Pharma4.0聚焦效率晋升与主动化普和,而Pharma5.0则描绘了一幅人机协同、绿色低碳的将来制药新图景。Pharma5.0的焦点... 2026-03-30 15:24-米兰·(milan)




























 粤公网安备 44011202003184号
粤公网安备 44011202003184号